(通訊員 吳疆鄂)7月6日,化學學院袁偉明課題組在化學國際知名期刊Angewandte Chemie International Edition(ACIE, 影響因子:12.959)上在線發表最新研究成果“Selective 1,2-Aryl-aminoalkylation of Alkenes Enabled by Metallaphotoredox Catalysis”,該成果突破了一級烷基自由基難以進行烯烴三組分共軛加成、偶聯串聯反應的瓶頸,為制備一系列具有重要生物活性的α-芳基取代的γ-氨基丁酸衍生物骨架提供了高效、簡潔合成路線。文章的第一作者為華中科技大學一年級博士研究生鄭松林,其中,化學院大三本科生廖子軒和李尉溶作為論文共同作者參與了該研究工作。華中科技大學為該論文唯一通訊單位,袁偉明研究員為該論文唯一通訊作者。
α-芳基取代的γ-氨基丁酸衍生物是一類重要的結構單元,在一些拮抗劑和藥物中表現出重要的生物活性(圖一)。傳統合成這類化合物的方法一般需要多步反應,且要使用一些強氧化劑、強堿或者活潑的有機金屬試劑,導致官能團兼容性以及原子和步驟經濟性較差。因此,開發更加簡潔、高效的方法合成此類結構骨架具有重要的研究意義。
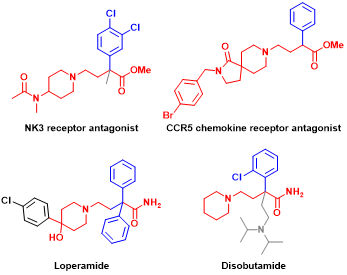
圖1:一些含有α-芳基取代的γ-氨基丁酸衍生物結構的拮抗劑和藥物
鎳/可見光氧化還原催化的烯烴的1,2-雙碳官能團化反應近年來得到了快速的關注(Chem. Sci. 2020, 11, 4051),該反應可以避免使用有機金屬試劑,取而代之的是使用廉價易得、溫和的烷基自由基前體作為碳親核試劑端,同時可見光的介入使得反應條件十分溫和,從而提高了該類反應的底物普適性、官能團兼容性以及原子和步驟經濟性。此外,相比于傳統的過渡金屬催化烯烴的雙碳化反應,金屬/可見光組合催化策略通過單電子氧化親核試劑端生成烷基自由基啟動反應,從而導致反應的區域選擇性發生完全翻轉。最近,Chu,Nevado,Molander和Aggarwal課題組分別報道了烯烴與芳基鹵化物和各類烷基自由基前體的三組分交叉偶聯反應。但是,這類反應都局限于二級和三級烷基自由基,而一級烷基自由基由于立體位阻小,活性高很容易直接與芳基鹵化物發生兩組分偶聯競爭反應,從而很難被應用于烯烴的共軛加成、偶聯三組分串聯反應中。
近日,華中科技大學的袁偉明課題組在鎳/光氧化還原催化下,以α-氨甲基三甲基硅烷為自由基前體成功實現了一級烷基自由基參與的烯烴1,2-雙碳官能團化反應。通過采用極性匹配增強效應以及形成穩定的一級氨基烷基自由基的策略有效抑制了兩組分偶聯以及Giese類型氫化副反應(圖2)。該反應條件十分溫和,無需外加任何堿或添加劑等,整個過程呈現氧化還原中性。反應具有很好的官能團兼容性和化學選擇性。該方法從廉價易得的原料出發,只需一步便能高效合成α-芳基取代的γ-氨基丁酸衍生物。
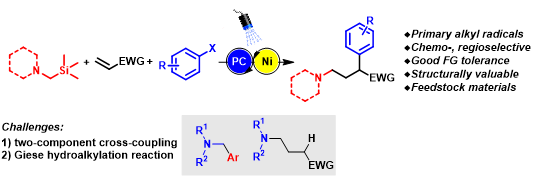
圖2:一級烷基自由基參與的烯烴1,2-雙碳官能團化反應
在該工作中,袁偉明課題組成功實現了一級烷基自由基參與的烯烴的1,2-雙碳官能團化三組分串聯反應,為快速合成高附加值的α-芳基取代的γ-氨基丁酸衍生物提供了一種簡潔、高效的合成方法,該方法有望在一些拮抗劑和藥物分子合成中發揮重要應用。
論文信息:
Selective 1, 2-Aryl-aminoalkylation of Alkenes Enabled by Metallaphotoredox Catalysis
Songlin Zheng, Zimin Chen, Yuanyuan Hu, Xiaoxiang Xi, Zixuan Liao, Weirong Li and Weiming Yuan*
Angewandte Chemie International Edition
https://www.onlinelibrary.wiley.com/doi/10.1002/anie.202006439
DOI: 10.1002/anie.202006439
