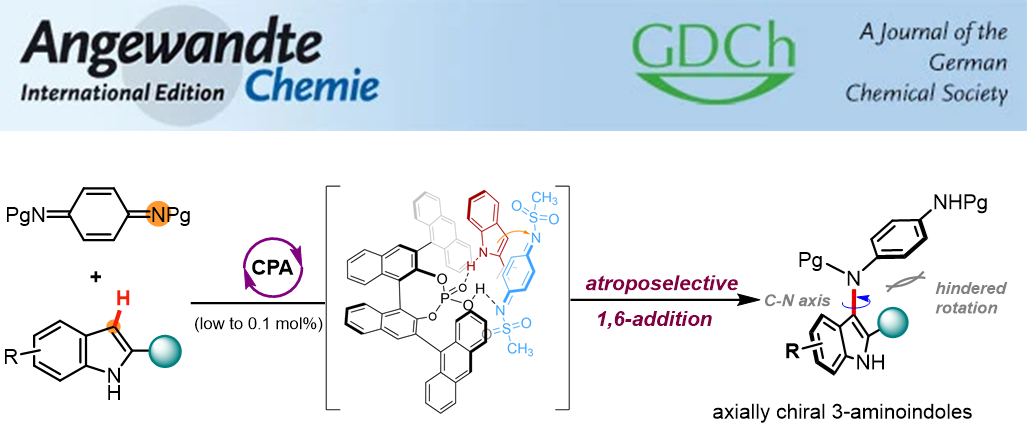
5月26日,國際期刊《德國應用化學》(Angewandte Chemie International Edition)在線刊發了化學與化工學院鐘芳銳教授和廖榮臻教授的最新合作研究成果“不對稱催化構建C-N軸手性氨基吲哚”(Catalytic Atroposelective Electrophilic Amination of Indoles, DOI: 10.1002/anie.202205159)。該論文發展了一種醌二亞胺與吲哚的阻轉選擇性1,6-加成新反應,制備了一系列含C-N手性軸的新穎氨基吲哚類分子。理論計算研究揭示了反應的機理,細胞毒性測試發現這類吲哚衍生物具有抗腫瘤活性。
手性吲哚衍生物在天然產物合成、藥物研發和材料科學等領域具有重要的用途。這類分子的現有合成研究主要集中在不對稱催化傅-克烷基化和芳基化反應,用于制備相應的中心手性和C-C軸手性吲哚衍生物。相比之下,受限于較低的構型穩定性,含C-N手性軸氨基吲哚分子的制備仍是研究難題。對此,鐘芳銳教授團隊在前期關于醌類化合物不對稱催化反應的研究基礎上,發現對苯醌二亞胺在手性質子酸催化下能與吲哚發生1,6-共軛加成反應。該反應模式與醌類化合物的經典1,4-加成顯著不同,醌二亞胺充當了一種高親電性的胺化試劑,而非已知的芳基化試劑。基于這一發現,鐘芳銳團隊通過選擇合適的手性磷酸催化劑,首次發展了阻轉選擇性的醌二亞胺1,6-加成反應,合成了一系列軸手性3-氨基吲哚類分子,催化劑用量低至千分之一,產物的光學純度高達98%。
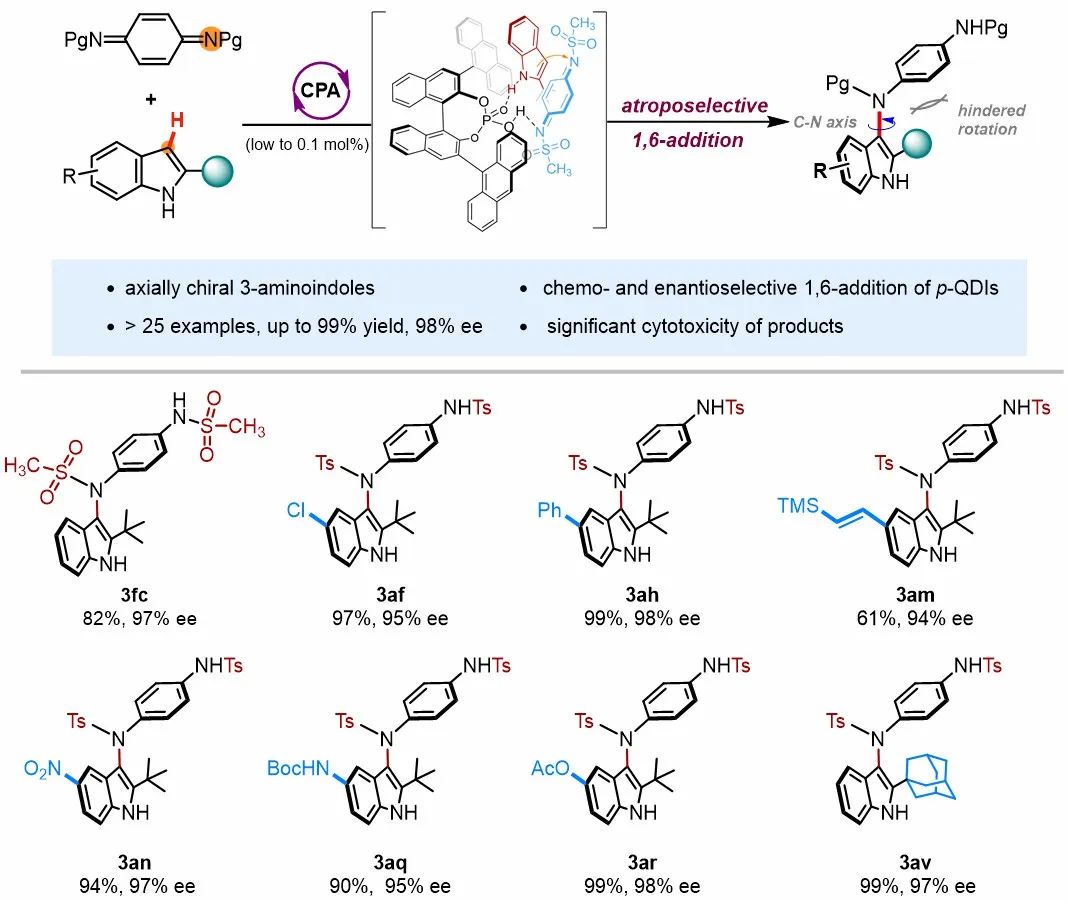
圖1 不對稱催化構建C-N軸手性氨基吲哚衍生物
廖榮臻教授團隊對該反應的機理進行了理論計算研究。結合自由基捕捉、自由基鐘、EPR譜等控制實驗,基于密度泛函理論模擬結果,提出上述1,6-共軛加成是通過離子型反應路徑進行。此外,與1,4-加成反應的過渡態和中間體能壘及其福井指數和軌道權重福井指數對比,該反應高度專一的1.6加成選擇性主要源自于醌二亞胺氮原子顯著的親電性以及過渡態和中間體較高的芳香性。
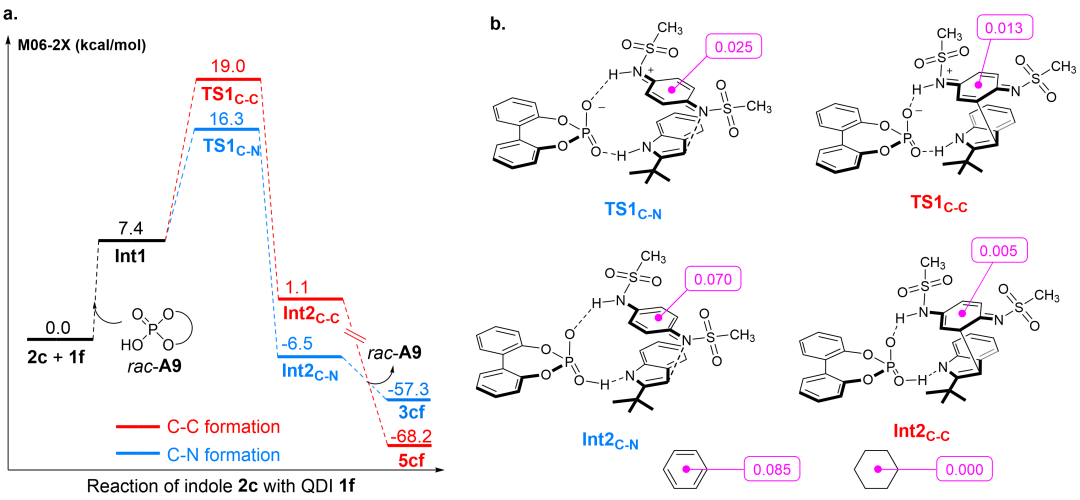
圖2 DFT理論計算解釋反應的區域選擇性
鑒于眾多吲哚衍生物往往表現出顯著的生物活性,研究團隊還測試了所合成的軸手性3-氨基吲哚的抗腫瘤活性。實驗結果顯示,其中三個化合物對于Hela細胞的IC50(半抑制濃度)值達到20μM左右,在相同條件下甚至優于臨床上常用的抗癌藥物伊立替康(irinotecan)和氟尿嘧啶(5-fluorouracil),表明這類新穎的軸手性3-氨基吲哚衍生物在藥物研發中有重要的應用前景。
我校為論文的唯一完成單位,鐘芳銳教授和廖榮臻教授是論文的共同通訊作者。生物活性測試由吳鈺周教授團隊合作完成。該論文第一作者為化學與化工學院2018級碩士研究生秦京陽(目前在CSC獎學金資助下于德國亞琛工業大學攻讀博士學位)。創新研究院2021級博士研究生周彤和化學與化工學院2019級碩士研究生周太平為論文的共同第一作者。該項工作得到了國家重點研發計劃(2018YFA0903500)、國家自然科學基金(21602067)和湖北科技創新重大專項(2019ACA125)資助。
文章鏈接:https://onlinelibrary.wiley.com/doi/epdf/10.1002/anie.202205159
